7 Antworten auf Fragen zur Impfstoffentwicklung
7 Antworten auf Fragen zur Impfstoffentwicklung
Die Entwicklung eines Impfstoffs, der eine gute Wirksamkeit und Verträglichkeit haben soll, ist ein zeit- und kostenintensiver Prozess. Das kann schon einmal bis zu 15 – 20 Jahre dauern und 300 – 800 Millionen Euro oder mehr kosten.1 Wir verraten 7 Fakten zur Impfstoffentwicklung!
Die notwendigen klinischen Studien bilden den wichtigsten Kostenfaktor im Entwicklungsprozess eines Impfstoffes:1
- Für eine Studie zur Sicherheit („extended safety“), für die etwa 10.000 – 60.000 Studienteilnehmer:innen erforderlich sind, summieren sich die Kosten auf 50 – 150 Millionen Euro.1
- Für eine Studie zur Wirksamkeit („efficacy“) sind zumindest ein paar Tausend Studienteilnehmer:innen nötig und es fallen Kosten von mindestens 50 Millionen Euro an.1
- Besondere Studien in Risikogruppen, wie z. B. chronisch Kranke oder Kinder, kosten mindestens 5 Millionen Euro.1
Wie lange es dauert, bis ein Impfstoff entwickelt ist, kann sehr unterschiedlich sein:
- Die frühere Entwicklung gängiger pädiatrischer Kombinationsimpfstoffe hat ca. 10 – 12 Jahre gedauert.1
- Die Entwicklung der Impfungen gegen humane Papillomviren (HPV) und Rotaviren hat jeweils etwa 15 Jahre gebraucht.1
- Die Entwicklung eines Impfstoffs gegen Varizellen sowie die der Influenza-Lebendimpfung dauerte jeweils 25 – 30 Jahre.1
- In Pandemiezeiten musste es schneller gehen: Die Impfstoffe gegen COVID-19 konnten dank neuer Plattform-Technologien2, früheren Erkenntnissen zu anderen Coronaviren und beschleunigten Abläufen und Verfahren3 binnen Monaten entwickelt und zugelassen werden2.
- Im Gegensatz dazu sind Impfstoffe gegen das Hepatitis-C-Virus (HCV) oder das humane Immundefizienz-Virus (HIV) bislang immer noch nicht verfügbar, obwohl seit über 30 Jahren daran geforscht wird.1
Warum ging die Entwicklung gängiger pädiatrischer Impfstoffe im Vergleich zu anderen Impfstoffen relativ schnell von statten? Der Grund: Es gab meist schon monovalente Präparate (Einzel-Impfstoffe) oder Ganzzell-Impfstoffe. Das Grundprinzip der Wirksamkeit des Impfstoffes stand hier aber schon länger fest. Sie wurden also nur als Kombinationsimpfstoffe oder Teilantigenimpfstoffe verbessert. Beispiele hierfür sind Toxoid-Impfstoffe gegen Tetanus (Wundstarrkrampf) und Diphtherie. Im Gegensatz dazu mussten für die Entwicklung „neuerer“ Impfstoffe, die z. B. gegen HPV und Rotaviren gerichtet sind, zuerst die schützenden Komponenten der Erreger identifiziert werden.
Darüber hinaus kamen bei der Herstellung mit molekularbiologischen Technologien andere Methoden zum Einsatz als bei früheren Impfstoffen: Die meisten viralen Impfstoffe werden schon seit den 1960er Jahren in Zellkulturen hergestellt. Dazu gehören z. B. die Impfstoffe gegen Masern, Polio, Tollwut und Röteln.1
Ein weiterer Grund für die längere Entwicklungsdauer neuerer Impfstoffe: Die Anforderungen für die klinische Prüfung haben sich in den letzten Jahrzehnten – mit besonderem Fokus auf Impfstoffsicherheit – sehr verändert.1
Wie kam es dann aber zu der relativ schnellen Zulassung von Impfstoffen gegen z. B. COVID-19? Die Impfstoffe gegen COVID-19 durchliefen die gleichen Entwicklungs- und Zulassungsschritte, wie andere Impfstoffe auch. Deutliche Optimierungen der Verfahrensabläufe haben jedoch zu einem Zeitgewinn bei der Entwicklung geführt. Dazu zählten z. B. eine frühe, kontinuierliche wissenschaftlich-regulatorische Beratung der Impfstoffentwicklung durch die Arzneimittelbehörden sowie ein Rolling-Review-Verfahren: Hier wurden schon während der klinischen Phase-III-Prüfung Datenpakete zur Vorab-Bewertung für die Zulassung vorgelegt. Zudem konnten die üblicherweise nacheinander ablaufenden klinischen Prüfungen kombiniert stattfinden.3
Ein kurzes, informatives Video zum Thema Impfstoffentwicklung in der Corona-Pandemie des Bundesministeriums für Bildung und Forschung (BMBF) haben wir für Sie hier verlinkt.
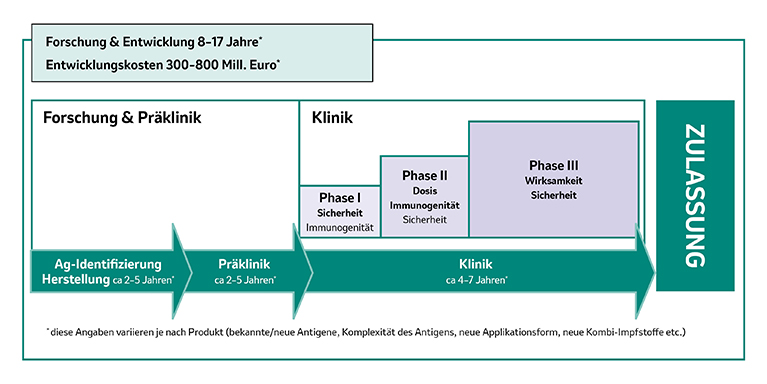
Abbildung 1: Phasen der Impfstoff-Entwicklung – Dauer und Kosten. Ag = Antigen. Modifiziert von MSD nach [1].
Es gibt eine ganze Reihe von wichtigen Faktoren, die bei der Frage, ob ein Impfstoff entwickelt wird oder eben nicht, eine entscheidende Rolle spielen:1
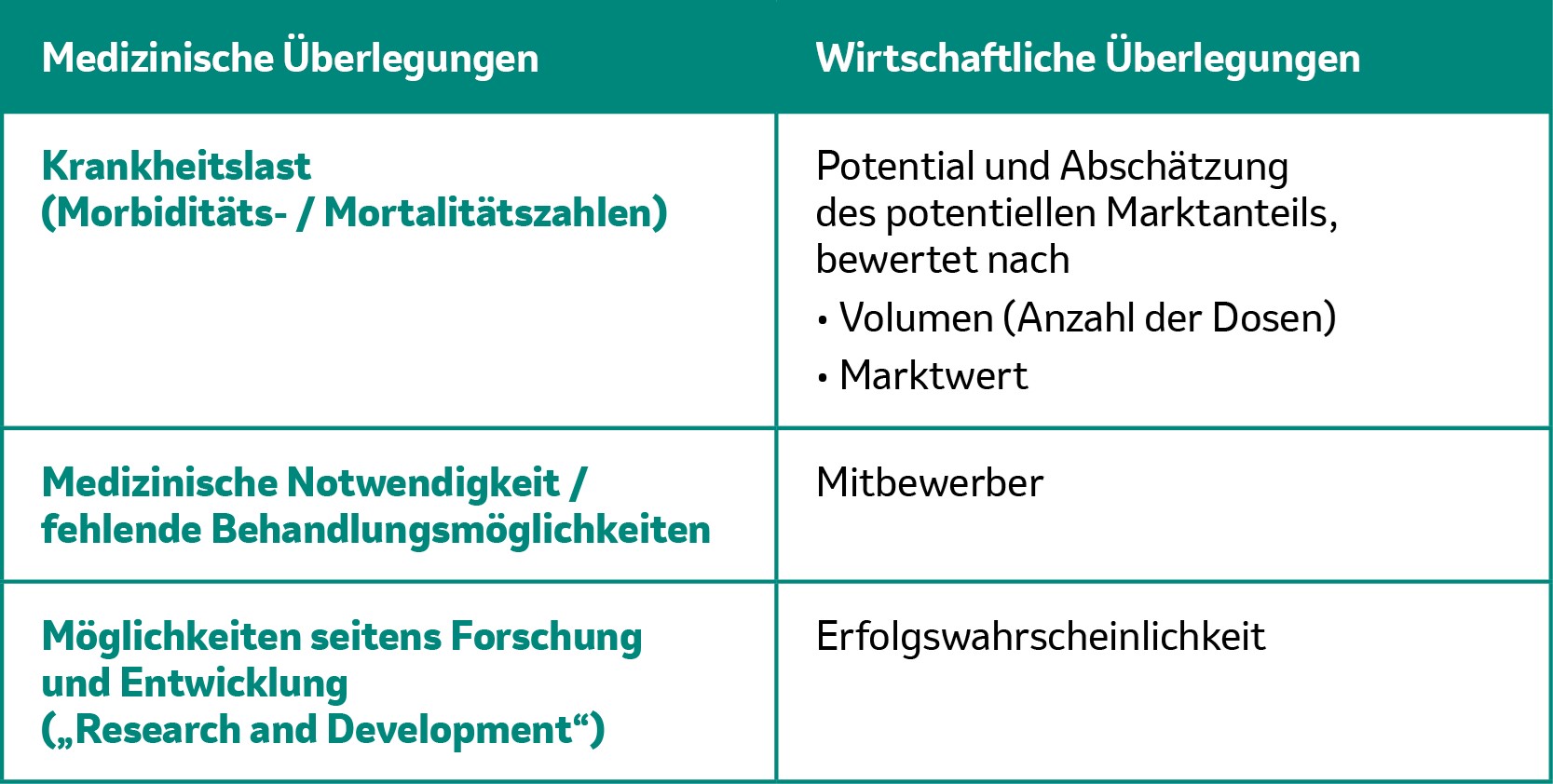
Tabelle 1: Entscheidende medizinische und wirtschaftliche Faktoren für die Impfstoffentwicklung. Modifiziert von MSD nach [1].
Heutzutage wird systematisch wissenschaftlich an die Impfstoffentwicklung herangegangen. Dies umfasst die Identifikation und genaue Charakterisierung des Erregers bzw. der Erregerbestandteile, einschließlich einer Analyse zur Identifikation der jeweiligen spezifischen Antigene, die eine schützende Immunantwort auslösen können.1
Die Impfstoffherstellung selbst lässt sich unterschiedlich angehen. Zunächst muss entschieden werden, ob es ein Lebendimpfstoff oder ein inaktivierter („Tot“)Impfstoff werden soll.1
Bei einem Lebendimpfstoff wird die gesamte Erregerstruktur, z. B. ein vollständiges, vermehrungsfähiges Virus als Impfantigen verwendet. Die Erreger werden dabei attenuiert, also in ihrer Virulenz so stark abgeschwächt, dass sie für einen gesunden Impfling keine Erkrankungsgefahr darstellen. Vorsicht ist hier jedoch bei immunsupprimierten Menschen geboten, da bei Lebendimpfstoffen von einem gesunden, funktionsfähigen Immunsystem ausgegangen wird.1
Bei Totimpfstoffen kann man mehrere Untertypen unterscheiden:1
- Beim Ganzzell-Impfstoff ist der Erreger als Gesamtheit erhalten, dabei jedoch inaktiviert.
- Beim Spalt-Impfstoff sind größere Teile eines zerstörten Erregers enthalten.
- Subunit-Impfstoffe enthalten nur noch bestimmte Antigene eines Erregers. Dazu gehören u. a. Toxoid-Impfstoffe z. B. gegen Tetanus und Diphterie oder Polysaccharidimpfstoffe (Mehrfachzucker aus den Bakterienkapseln, etwa von Pneumokokken).
Bei den Vektor-Impfstoffen dient ein abgeschwächtes (attenuiertes) Virus als Transportmittel (Vektor) für einen ungefährlichen Teil der Erbinformation eines Erregers in wenige Körperzellen.2 Das Vektor-Virus kann dabei vermehrungsfähig oder auch nicht vermehrungsfähig sein und überträgt den Bauplan für ein oder auch mehrere Antigene.4
mRNA-Impfstoffe enthalten Teile der Erbinformation eines Virus in Form einer Boten-RNA (messenger-RNA; mRNA). Um die Aufnahme der mRNA in die Zellen möglich zu machen, wird sie mit Lipidstoffen, also kleinen Fetttröpfchen umhüllt. Es entstehen sogenannter mRNA-Lipidnanopartikel. Nach der Injektion in den Muskel verschmelzen diese mit der Zellmembran der Muskelzellen, wodurch die mRNA in die Zellen gelangt. Die Nanopartikel sind nicht zellschädigend und stellen keine Gefahr für den Körper dar. In den Zellen wird die mRNA als Vorlage genutzt, um die darin codierten Virusproteine zu produzieren. Komplette, vermehrungsfähige Viren können hier jedoch nicht entstehen, da nur einzelne Bestandteile des Virus gebildet werden. Diese neu gebildeten, ungefährlichen Virusproteine dienen nun als Antigene und aktivieren so das Immunsystem.5
Darüber hinaus gibt es mehrere Methoden zur Auslösung oder Verbesserung einer schützenden Immunantwort nach Impfung. Dazu zählen z. B. die Bindung von Antigenen an Trägerproteine, die Verwendung von immunstimulierenden Adjuvantien (Hilfsstoffen), die Verwendung von Virus-ähnlichen Partikeln („Virus-Like Particles“, VLP) sowie die so genannte „reverse Vakzinologie“ zur Identifikation von potentiellen Impfstoffantigenen.1
Für Impfstoffe gelten genau wir für neue Arzneimittel – unabhängig vom Wirkstoff – immer standardisierte Entwicklungsgrundsätze. Gibt es am Anfang im Labor noch 10.000 Kandidatensubstanzen, dann bleiben aufgrund der hohen Qualitätsanforderungen vielleicht noch 250 davon übrig, die in die präklinische Phase gehen. Am Ende bleiben vielleicht 5, die in die klinische Entwicklung gehen – und auch hier bedeutet das keine automatische Zulassung.1
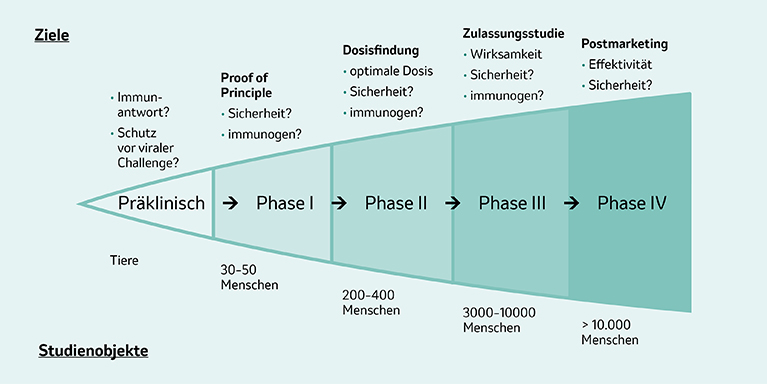
Abbildung 2: Schematischer Ablauf der Phasen und Zahl der benötigten Studienteilnehmer:innen bei der Impfstoffentwicklung. Modifiziert von MSD nach [1].
Vor Beginn einer klinischen Studie, werden erste Information zur Wirksamkeit, Immunogenität (Fähigkeit, eine Immunantwort auszulösen) und Sicherheit des verwendeten Antigens tierexperimentell erhoben. Hier geht es vor allem um die Dosis, die Impfstoffzusammensetzung, ggf. um Zusatz von Wirkungsverstärkern (sogenannte Adjuvantien/Immunmodulatoren) und den optimalen Verabreichungsweg (intradermal, subkutan, intramuskulär). Allerdings sind die Etablierung von Tiermodellen und generell auch die Übertragung präklinischer Ergebnisse auf den Menschen nicht immer einfach und auch nicht 1:1 möglich.1
In Phase-I-Studien werden Impfstoffe erstmals am Menschen („first in human“) geprüft: Man tastet sich anhand einer geeigneten Startdosis und einer relativ kleinen Probandenzahl (z. B. 30) an die Eigenschaften des Impfstoffkandidaten heran. Das vorrangige Ziel ist dabei Erkenntnisse zur Sicherheit und Verträglichkeit zu erhalten.1
Zusätzlich:
- werden vorläufige Daten zur Immunogenität erhoben.1
- wird die gewählte Dosis und Applikationsart geprüft und ggf. angepasst.1
- werden bei lebend-attenuierten Impfstoffen ggf. auch erste Informationen zu Erregerausscheidung, Übertragbarkeit der Impfviren auf andere Personen (Transmission) und genetischer Stabilität erhoben.1
- wird grundsätzlich eine Basis geschaffen, um nachfolgende eindeutigere (definitivere) und größere Studien optimal planen zu können.1
Bei der Erstanwendung am Menschen muss die Impfdosis (Antigenmenge bzw. die Verwendung von Adjuvantien) so gewählt werden, dass sie verträglich genug ist (lokal und systemisch), um eine Gefährdung möglichst zu vermeiden, aber dennoch immunogen genug, um die erwünschte Immunantwort nachweisbar auszulösen.1
So werden in Phase I vorwiegend sehr häufige Nebenwirkungen erfasst.1
Phase-II-Studien haben meist mehrere 100 Studienteilnehmer:innen aus der Zielpopulation. Ziel dieser Studien ist es die Immunogenität und Sicherheit des Testimpfstoffs zu bestätigen. Dabei geht es besonders um die Dosis-, Applikations- und Impfschema-Optimierung für große Phase-III-Studien. Zudem wird der Einfluss von unterschiedlichen Variablen auf die Immunantwort untersucht, z. B. werden Alter, Geschlecht, vorher bestehende Antikörper und der Prozentsatz der Responder erhoben.1
Phase-I- und Phase-II-Studie dauern jeweils etwa 1 – 1 ½ Jahre und können getrennt oder als kombinierte Phase-I/II-Studien durchgeführt werden.1
Die klinische Phase III kann bis zu 4 Jahre dauern. In dieser Phase nehmen bereits einige Tausend freiwillige Teilnehmer:innen an den Impfstudien teil. Phase-III-Studien werden zum Teil auch als „Zulassungsstudien“ bezeichnet. Dabei geht es um den Nachweis eines positiven Nutzen-Risiko-Profils – also um den bestmöglichen Schutz bei vertretbarem Risikoprofil.1
Phase-III-Studien dienen der Untersuchung von Sicherheit und Wirksamkeit eines Impfstoffs für die jeweilige Indikation und Zielpopulation. Außerdem wird durch sogenannte „lot to lot consistency“-Studien die Konsistenz in der Herstellung von Charge zu Charge klinisch überprüft.1
Die klinische Phase IV umfasst die sogenannten Postmarketing-Studien für den bereits zugelassenen Impfstoff. Für gewöhnlich werden darin mehr als 10.000 Teilnehmer:innen eingeschlossen. Hierbei handelt es sich z. B. um Studien zum Sicherheitsprofil, denn: Seltenere Nebenwirkungen können auch mit mehreren Tausend Teilnehmer:innen in Phase-III-Studien nicht sicher erfasst werden.1 Es kann daher sinnvoll sein, ein bereits zugelassenes Medikament bei Patient:innen mit bestimmten Eigenschaften noch einmal gezielt zu untersuchen, etwa in einer besonderen Altersgruppe oder bei Patient:innen mit bestimmten Vorerkrankungen.6
Unter Pharmakovigilanz versteht man Tätigkeiten, die sich mit der Aufdeckung, Bewertung, Prävention und dem Verstehen von Nebenwirkungen oder von anderen Arzneimittel-bezogenen Problemen befassen.7 In diesem Zuge können klinische Phase-IV-Studien u. a. als nicht-interventionelle Studien oder als Fall-Kontroll-Studien durchgeführt werden. Dabei wird das Sicherheitsprofil nach Zulassung des Impfstoffs ständig durch den Zulassungsinhaber und die zuständige Behörde überwacht.1
Das behördliche Zulassungsverfahren überprüft anhand der regulatorischen Angaben:1
- Daten zur Herstellung
- Präklinische Daten
- Klinische Daten
- Informationen zur Pharmakovigilanz
- Informationen zu den Impfstoffantigenen
- Informationen zu allen anderen Inhaltsstoffen
Ein Arzneimittel wird zugelassen, wenn es ein positives Nutzen-Risiko-Verhältnis zeigt.1
Impfstoffe gehören dabei zu den Chargenfreigabe-pflichtigen Arzneimitteln: Jede Charge muss von einem staatlichen Arzneimittelkontrolllabor („Official Medicines Control Laboratory“ – OMCL) eines EU- bzw. EWR- (Europäischer Wirtschaftsraum-)Landes geprüft und freigegeben werden.1
Solang ein Produkt auf dem Markt ist, werden auch laufend Nebenwirkungsmeldungen evaluiert. Dazu ist es für den Zulassungsinhaber verpflichtend, der Behörde regelmäßige Sicherheitsberichte – sogenannte „Periodic Safety Update Reports“ (PSUR) – vorzulegen.1
Eventuell neu auftretende Risiken müssen anlassbezogen und umgehend beurteilt werden. Zudem müssen Risiko-minimierende Maßnahmen gesetzt werden. Das können beispielsweise Änderung der Produktinformation oder Informationsschreiben an Ärzte und Ärztinnen sein.1
Für Sie interessant:
Warum zählen Impfungen zu den wichtigsten medizinischen Maßnahmen? Welche Impfstoffarten gibt es und welche Applikationsstellen sind möglich? Mehr darüber hier!
Quellen
- Wiedermann U., et al. Entwicklung von Impfstoffen. Österreichische Ärztezeitung Nr. 23 – 24. 15.Dezember 2017.
- Bundeszentrale für gesundheitliche Aufklärung (BzgA), Robert Koch-Institut (RKI), Bundesministerium für Gesundheit. Das Impfbuch für alle. Abrufbar unter: https://shop.bzga.de/das-impfbuch-fuer-alle/ [eingesehen am 02.10.2024].
- Paul-Ehrlich-Institut. Coronavirus FAQ. Entwicklung und Zulassung. Online verfügbar unter: https://www.pei.de/DE/service/faq/coronavirus/faq-coronavirus-node.html [eingesehen am 02.10.2024].
- Bundesministerium für Bildung und Forschung. Coronavirus. Corona-Impfstoffe im Vergleich: Unterschiede der Impfstoffarten. Stand: 15.05.2024. Online verfügbar unter: https://www.bmbf.de/bmbf/shareddocs/kurzmeldungen/de/coronavirus-impfstoffe-im-vergleich.html [eingesehen am 02.10.2024].
- Robert Koch-Institut (RKI). Impfstofftypen. Stand: 26.09.2024. https://www.rki.de/SharedDocs/FAQ/COVID-Impfen/FAQ_Liste_Impfstofftypen.html [eingesehen am 02.10.2024].
- Bundesministerium für Bildung und Forschung. Klinische Forschung. Wie funktionieren klinische Studien? Abrufbar unter: https://www.gesundheitsforschung-bmbf.de/de/wie-funktionieren-klinische-studien-6877.php [eingesehen am 25.10.2024].
- Paul-Ehrlich-Institut (PEI). Pharmakovigilanz (human). Abrufbar unter: https://www.pei.de/DE/arzneimittelsicherheit/pharmakovigilanz/pharmakovigilanz-node.html [eingesehen am 02.10.2024].
DE-NON-03961 10/24